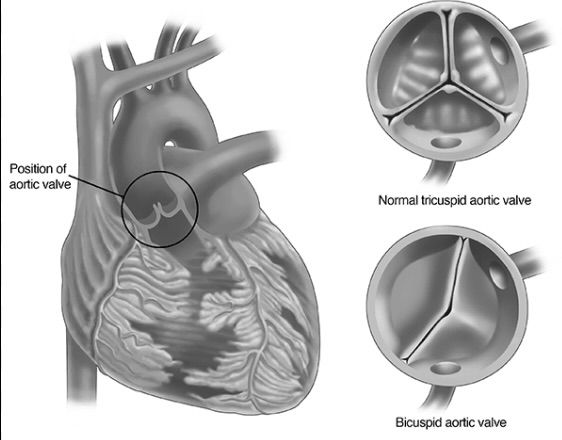
A bicuspid aortic valve is the most common congenital abnormality of the cardiac valve apparatus, in which two leaflets are formed instead of the normal three. This feature arises during early fetal development due to incomplete separation of the valve primordia. In most cases, fusion occurs between the right and left coronary leaflets, which determines the characteristic morphology of the valve. This anomaly may remain asymptomatic for a long time, yet over time it creates conditions for changes in the function of the heart and the ascending aorta.
Because of its structural characteristics, a bicuspid valve opens and closes differently from a normal tricuspid valve. This leads to an asymmetric blood flow through the aortic valve, formation of vortices, and increased local stress on the aortic wall. Such hemodynamic effects may gradually cause dilation of the aortic root and ascending aorta. In addition, some patients have congenital connective tissue features of the aortic wall that make it more susceptible to stretching. Therefore, a bicuspid valve is considered not only a valvular abnormality but also a condition associated with an increased risk of aortopathy.
Over time, valvular changes may lead to the development of aortic stenosis or aortic regurgitation. In stenosis, the leaflets become thickened, rigid, and open poorly, making it more difficult for the heart to eject blood. In regurgitation, the leaflets do not close completely, causing part of the blood to flow back into the left ventricle. Both conditions may progress and lead to shortness of breath, fatigue, reduced exercise tolerance, and other symptoms. Another risk is infective endocarditis, as the altered surface of the leaflets facilitates bacterial adherence.
Beyond valvular dysfunction, significant attention is given to dilation of the ascending aorta. In some cases, the aortic diameter may gradually increase to a size at which the risk of dissection becomes significant. This condition is extremely dangerous and can develop suddenly, making timely monitoring crucial.
Diagnosis of a bicuspid aortic valve is based primarily on echocardiography. This simple, safe, and informative method enables assessment of leaflet morphology, severity of stenosis or regurgitation, left ventricular dimensions, and parameters of the ascending aorta. Regular echocardiography is especially important, as even asymptomatic changes may progress, and only dynamic monitoring allows timely detection of increasing aortic dimensions or deterioration of valve function. For this reason, cardiology visits should be regular, allowing adjustment of the follow-up plan, determination of optimal examination frequency, and control of blood pressure, activity, and lifestyle.
In cases of significant valvular dysfunction or marked aortic dilation, surgical treatment is considered. Depending on the situation, this may involve open valve replacement or aortic reconstruction, or modern catheter-based techniques. Among minimally invasive interventions is a procedure in which the valve is implanted through a vascular access without opening the chest. This method allows placement of a new valve with minimal trauma and quick recovery, which is especially important for patients who have contraindications to open surgery. The prosthesis is delivered through the femoral artery or another vessel and expanded inside the patient’s own dysfunctional valve. This approach ensures proper valve function without the need for cardiac arrest or prolonged rehabilitation.
The choice of procedure depends on the patient’s age, aortic anatomy, degree of leaflet calcification, left ventricular function, and other factors. Regardless of the method, the goal is to restore normal blood flow, prevent progression of heart failure, and reduce the risk of dangerous aortic complications.
Thus, a bicuspid aortic valve is a congenital condition combining structural valve abnormalities, unique hemodynamics, and a tendency toward ascending aortic dilation. This combination requires long-term observation, regular cardiology follow-up, and periodic imaging of the heart and vessels. Timely diagnosis and an appropriate treatment strategy help prevent complications, ensure a stable course of the condition, and maintain quality of life.
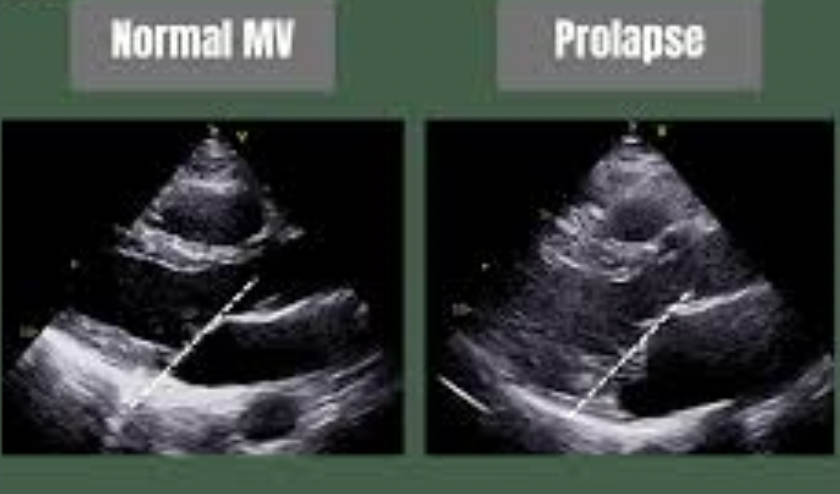
Mitral valve prolapse is one of the most common conditions of the cardiac valve apparatus, in which the mitral leaflets bulge into the left atrium during systole. This feature arises due to alterations in the connective tissue structure of the leaflets or the chordae that support the valve. Mitral valve prolapse may be congenital, associated with connective tissue characteristics, or acquired, forming over time under the influence of various factors affecting the valve and its supporting structures.
The structural basis of prolapse lies in excessive leaflet mobility and elongation of the supporting chordae. As a result, the leaflets may close incompletely or with delay, leading to excessive bulging toward the atrium. Some patients exhibit thickening and increased rigidity of the leaflets, which also affects their elasticity. Despite these changes, many individuals with mitral valve prolapse remain asymptomatic for years and are unaware of the condition.
However, under certain circumstances, prolapse may be accompanied by mitral regurgitation, when part of the blood returns from the left ventricle into the atrium. This regurgitation may gradually increase, causing palpitations, irregular heartbeats, fatigue, and reduced exercise tolerance. Some patients report chest discomfort not related to ischemia, explained by features of autonomic regulation and stretching of valve structures. Occasional episodes of dizziness or brief weakness may also occur due to autonomic nervous system fluctuations.
The connective tissue of the mitral valve and its chordae is susceptible to age-related changes, mechanical stress, and chronic processes. Over time, these factors may lead to chordal elongation or weakening and an increase in the degree of prolapse. In some situations, chordae may rupture, causing a sudden increase in regurgitation and requiring urgent intervention. Among the complications of prolapse are cardiac arrhythmias, which may occur regardless of the severity of regurgitation and manifest as palpitations, rapid heartbeat episodes, and a sense of discomfort.
There is also an increased risk of infective endocarditis, since the altered leaflet surface is more vulnerable to bacterial adhesion. Although such cases are rare, the risk increases when significant regurgitation or structural changes are present.
Diagnosis of mitral valve prolapse is based on echocardiography, which provides visualization of leaflet displacement, assessment of leaflet thickness and mobility, and evaluation of regurgitation severity. Echocardiography is the key method for follow-up, enabling detection of progression and timely adjustment of management. Regular cardiology visits are essential for monitoring symptoms, assessing cardiac function, choosing examination frequency, and adapting treatment strategy.
In most cases, mitral valve prolapse does not require specific treatment and is managed with observation. However, if regurgitation increases, medical therapy may be used to reduce cardiac load and improve symptoms. When mitral insufficiency becomes significant, surgical treatment is considered. The preferred approach is mitral valve repair, which preserves the native leaflets and restores proper coaptation. This surgery involves reinforcing the leaflets, shortening or replacing chordae, and adjusting the size of the annulus. In some cases, valve replacement is performed if reconstruction is not feasible.
Modern minimally invasive methods include devices that reduce regurgitation by approximating the leaflets through vascular access. This approach is suitable for patients who cannot undergo traditional surgery and provides improved hemodynamics without open-chest intervention.
Mitral valve prolapse requires careful, long-term observation. Although it often has a benign course, regular assessment of valve condition, cardiac function, and regurgitation severity is crucial. Early detection of changes helps prevent complications, reduce the risk of heart failure progression, and maintain a high quality of life.
It is important to understand that a person may live for years without knowing they have a valvular disorder. Often, symptoms appear only when irreversible changes have already formed in the heart. Therefore, timely cardiology consultation and simple, accessible diagnostic testing are essential. Take care of your heart today — it is the best way to preserve your health and extend your quality of life.
Двухстворчатый аортальный клапан и пролапс митрального клапана – что это? Как с этим жить? И как их найти, а главное зачем?
Двухстворчатый аортальный клапан является наиболее распространённой врождённой аномалией клапанного аппарата сердца, при которой вместо трёх нормальных створок формируются две. Такая особенность возникает в период раннего развития плода из-за неполного разделения зачатков клапана. Чаще всего сращение происходит между правой и левой коронарными створками, что определяет характерную морфологию клапана. Эта аномалия может долгое время не проявляться, однако со временем создаёт условия для изменений в работе сердца и восходящей аорты.
Из-за особенностей строения двухстворчатый клапан открывается и закрывается иначе, чем нормальный трёхстворчатый. Это приводит к тому, что поток крови через аортальный клапан становится несимметричным, образуются вихревые зоны, усиливается локальное давление на стенку аорты. Такое влияние может постепенно вызывать расширение корня и восходящей аорты. Кроме того, у части пациентов имеются врождённые особенности соединительной ткани стенки аорты, из-за которых она более подвержена растяжению. Поэтому двухстворчатый клапан рассматривается не только как клапанная аномалия, но и как состояние, связанное с повышенным риском формирования аортопатии.
Со временем клапанные изменения могут приводить к развитию аортального стеноза или аортальной регургитации. При стенозе створки становятся плотными, ригидными и хуже открываются, что затрудняет выброс крови из сердца. При регургитации створки смыкаются неплотно, из-за чего часть крови возвращается обратно в левый желудочек. Оба состояния могут прогрессировать и приводить к появлению одышки, утомляемости, снижения толерантности к нагрузке и других симптомов. Ещё одним риском является инфекционный эндокардит, так как изменённая поверхность створок облегчает фиксацию бактерий.
Кроме клапанной дисфункции значительное внимание уделяется расширению восходящей аорты. В ряде случаев диаметр аорты может увеличиваться постепенно, достигая размеров, при которых возникает угроза её расслоения. Это состояние является крайне опасным и может развиваться внезапно, поэтому своевременное наблюдение играет ключевую роль.
Диагностика двухстворчатого аортального клапана основана прежде всего на эхокардиографии. Это простой, безопасный и информативный метод, который позволяет оценить строение створок, степень стеноза или регургитации, размеры левого желудочка и параметры восходящей аорты. Регулярное ЭХО особенно важно, потому что даже бессимптомные изменения могут прогрессировать, и только динамическое наблюдение позволяет вовремя увидеть тенденцию к увеличению аорты или ухудшению функции клапана. По этой причине посещение кардиолога должно быть регулярным. Это позволяет своевременно корректировать план наблюдения, подбирать оптимальную частоту исследований, контролировать давление, нагрузку и образ жизни.
При выраженной клапанной дисфункции или значительном расширении аорты рассматривается хирургическое лечение. В зависимости от конкретной ситуации выполняется либо открытая операция по замене клапана или реконструкции аорты, либо современные катетерные методики. Среди малоинвазивных вмешательств используется процедура, при которой клапан устанавливают через сосудистый доступ без разреза грудной клетки. Этот метод позволяет имплантировать новый клапан с минимальной травмой и быстрым восстановлением, что особенно важно для пациентов, имеющих противопоказания к открытой операции. Метод доставляет протез через бедренную артерию или другой сосуд и развёртывает его внутри собственного поражённого клапана. Такой подход позволяет обеспечить полноценную работу клапана без необходимости остановки сердца и длительной реабилитации.
Выбор типа операции зависит от возраста пациента, анатомии аорты, степени кальцификации створок, функции левого желудочка и других факторов. Но независимо от метода, целью вмешательства является восстановление нормального кровотока, предотвращение прогрессирования сердечной недостаточности и снижение риска опасных осложнений со стороны аорты.
Таким образом, двухстворчатый аортальный клапан представляет собой врождённое состояние, сочетающее аномалию структуры клапана, особую гемодинамику и склонность к расширению восходящей аорты. Такое сочетание требует долгосрочного наблюдения, регулярных визитов к кардиологу и периодической визуализации сердца и сосудов. Своевременная диагностика и правильный выбор тактики лечения позволяют избежать осложнений, обеспечить стабильное течение заболевания и сохранить качество жизни пациента
Пролапс митрального клапана представляет собой одно из наиболее распространённых состояний клапанного аппарата сердца, при котором створки митрального клапана прогибаются в полость левого предсердия во время систолы. Такая особенность возникает вследствие изменений в структуре соединительной ткани створок или хордов, удерживающих клапан. Пролапс может быть врождённым, связанным с особенностями формирования соединительной ткани, или приобретённым, формируясь со временем под воздействием различных факторов, влияющих на клапан и его опорные структуры.
Структурная основа пролапса заключается в избыточной подвижности створок и удлинении поддерживающих хорд. При этом створки могут смыкаться неплотно или смыкаться с задержкой, что приводит к излишнему прогибанию в сторону предсердия. Для ряда пациентов характерно уплотнение и утолщение створок, что также влияет на их эластичность. Несмотря на описанные изменения, значительная часть людей с пролапсом митрального клапана длительное время не испытывает никаких симптомов и не подозревает о наличии данной особенности.
Однако при определённых условиях пролапс может сопровождаться негерметичностью клапана, когда часть крови возвращается из левого желудочка обратно в предсердие. Эта митральная регургитация может постепенно увеличиваться, приводя к появлению ощущения сердцебиения, перебоев в работе сердца, утомляемости и снижению переносимости физической нагрузки. В некоторых случаях пациенты отмечают боли в грудной клетке, не связанные с ишемией, что объясняется особенностями нервной регуляции и растяжением структур клапана. Дополнительно возможны эпизоды головокружения и кратковременной слабости, что связано с изменениями тонуса вегетативной нервной системы.
Узлы соединительной ткани митрального клапана и его хорд подвержены возрастным изменениям, механическим нагрузкам и хроническим процессам. Со временем эти изменения могут приводить к удлинению или ослаблению хорд и увеличению степени пролапса. В некоторых ситуациях хорды могут разрываться, что вызывает резкое усиление регургитации и требует неотложного вмешательства. Среди осложнений пролапса также рассматриваются нарушения ритма сердца, которые могут возникать как при отсутствии выраженной регургитации, так и при её наличии. Они проявляются ощущением перебоев, эпизодами учащённого сердцебиения и чувством внутреннего дискомфорта.
Отдельное внимание уделяется повышенному риску инфекционного поражения клапана, поскольку изменённая поверхность створок более уязвима для фиксации бактерий. Хотя подобные случаи встречаются редко, риск увеличивается при наличии значимой регургитации или сопутствующих структурных изменений.
Диагностика пролапса митрального клапана основана на эхокардиографии, которая позволяет визуализировать степень прогибания створок, оценить толщину и подвижность клапанных элементов, а также определить выраженность митральной регургитации. ЭХО является ключевым методом наблюдения, поскольку позволяет отслеживать динамику изменений и вовремя выявлять прогрессирование состояния. Регулярные визиты к кардиологу необходимы для контроля симптомов, оценки функции сердца, подбора частоты обследований и своевременной коррекции тактики ведения пациента.
В большинстве случаев пролапс митрального клапана не требует специального лечения и ограничивается наблюдением. Однако при нарастании регургитации может потребоваться медикаментозная терапия, направленная на снижение нагрузки на сердце и улучшение самочувствия. Когда митральная недостаточность достигает значительной степени, рассматриваются варианты хирургического лечения. Наиболее предпочтительным подходом является пластика митрального клапана, позволяющая сохранить собственные створки и восстановить нормальный механизм смыкания. Эта операция предусматривает укрепление створок, укорочение или замену хорд и корректировку размеров клапанного кольца. В ряде случаев выполняется протезирование клапана, если реконструкция невозможна.
Современные малоинвазивные методы предусматривают использование специальных систем, позволяющих уменьшить регургитацию путём сближения створок через сосудистый доступ. Такой подход применяется у пациентов, которым противопоказана классическая хирургия, и обеспечивает улучшение гемодинамики без необходимости открытого вмешательства.
Пролапс митрального клапана является состоянием, требующим внимательного и долгосрочного наблюдения. Несмотря на то, что он часто протекает благоприятно, важно регулярно оценивать состояние клапана, функцию сердца и выраженность регургитации. Своевременное выявление изменений позволяет предотвратить осложнения, снизить риск прогрессирования сердечной недостаточности и сохранить качество жизни пациента.
Важно понимать, что человек может годами не подозревать о наличии клапанной патологии. Часто признаки появляются только тогда, когда в сердце уже формируются необратимые изменения. Поэтому своевременный визит к кардиологу и простое, доступное обследование имеют решающее значение. Позаботьтесь о своём сердце сегодня — это лучший способ сохранить здоровье и продлить качество жизни.